
조직 고정 과정과 고정제의 특성

조직 고정의 목적은 세포와 조직 성분을 “생물과 같은 상태”로 보존하고 이 조직을 얇고 염색된 절편으로 분리하기 위한 방식입니다. 1물론 고정 이후 단계 동안 세포와 조직 성분의 형태와 구성에는 상당한 변화가 있으며 이상적인 “생물과 같은 상태”와는 꽤 거리가 멀어집니다.
고정의 중요성
조직 고정의 목적은 세포와 조직 성분을 “생물과 같은 상태”로 보존하고 이 조직을 얇고 염색된 절편으로 분리하기 위한 방식입니다. 1물론 고정 이후 단계 동안 세포와 조직 성분의 형태와 구성에는 상당한 변화가 있으며 이상적인 “생물과 같은 상태”와는 꽤 거리가 멀어집니다. 하지만 조심히 다루면 패턴을 관찰할 수 있고, 형태학적 및 화학적 변화를 알 수 있으며, 비교 가능한 일정한 화학적 및 물리적 특성들을 조직 절편 내에 관찰할 수 있습니다. 이렇게 진행한 관찰 내용들은 끊임없이 변화하는 환경을 특정 시점에 “고정”시켜 볼 수 있으며2, 조직병리학적 진단을 가능하게 해줍니다.
아울러 실질적으로 고정과정은 조직에 혈액 공급이 끊기는 즉시 시작되는 변성 과정을 저지하는 것이라서, 기관의 Membrane 파괴되면서 분비되는 세포내 Enzyme에 의해 조직 변성 일으키는 자가용해와 그리고 시료에 이미 존재할 수 있는 미생물에 의해 일어나는 세균 분해나 부패는 반드시 막아야 하는 과정입니다. 수용성 물질의 손실과 확산은 이러한 성분들의 침전이나 응고를 통해서 또는 다른 불용성 구조적 성분들과의 교차결합을 통해서 최대한 피해야 합니다. 조직들은 고온의 왁스 침윤을 포함한 조직 처리 과정에서의 해로운 영향으로부터 보호되어야 하지만 중요한 것은 조직이 염색 시약과 항체 및 DNA, RNA Probe를 포함한 다른 시약에 대한 반응성을 유지해야 합니다. 1, 2
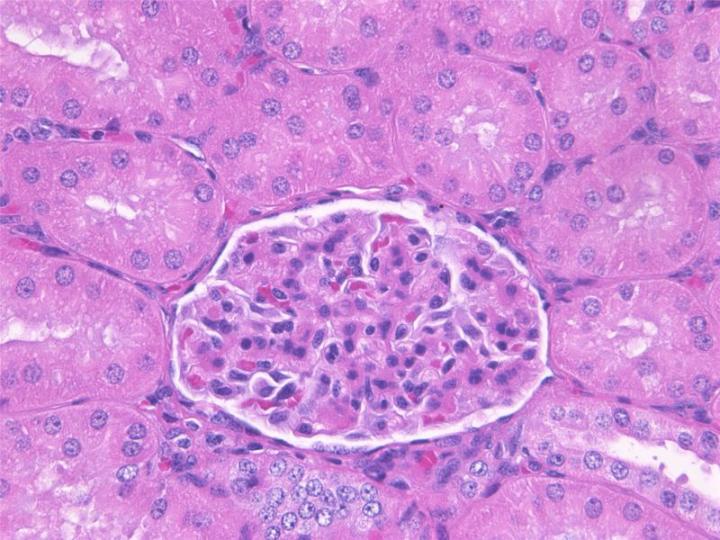
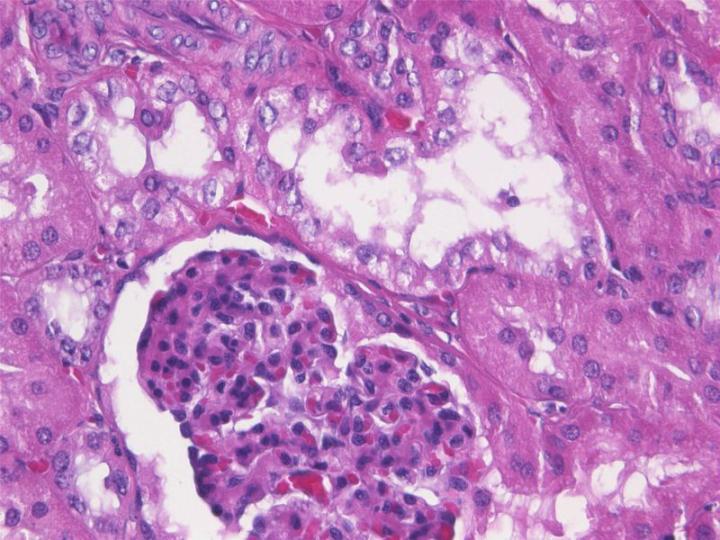
고정제 이용시 일반적으로 수용성 환경인 조직에서 초반에 많은 변화를 일으킨다는 것을 아는 것이 중요합니다. 이는 다양한 구성 요소들의 수축, 팽창, 경화 등이 포함된다. 이러한 초기 효과에도 불구하고, 조직은 비수용성 환경에 놓일 때 처리 과정 중 추가적인 변화가 일어납니다. 2 예를 들어, 10% 포르말린 완충 용액으로 고정하면 조직샘플에 약간의 팽창을 유발합니다. 하지만 처리 과정 중 샘플은 20~30% 정도 수축될 수 있습니다. 3또한 특정 고정제의 사용은 각각의 성분들이 다양한 조직화학적, 면역조직화학적 시약들에 의해 얼마만큼 염색정도에 영향을 줍니다. 4그러므로 특정 고정제의 조직에 대한 영향은 필수 요소들을 나타내기 위해 조직이 처리되고, 절편되고, 염색된 후에 평가되어야 합니다.
고정의 종류
조직의 고정은 화학적 또는 물리적인 방법으로 달성될 수 있습니다. 물리적 방법에는 가열, 극초단파 고정, 냉동보존(동결건조) 등이 있습니다. 가열 고정은 조직 샘플에는 거의 사용되지 않으며 미생물 샘플에 국한되어 사용됩니다. 하지만 가열 고정의 한 형태라고 여길 수 있는 극초단파 고정은 현재 일반적인 실험실에서 널리 사용되고 있으며 이는 Part 5. 에서 다시 설명 드리겠습니다. 냉동보존은 주로 동결건조의 형태로 조직화학법에서 일부 응용이지만, 대게 진단 조직 검체에는 사용되지 않습니다.2
화학적 고정은 일반적으로 샘플을 고정제에 담그거나 (침수고정) 작은 동물이나 폐와 같은 일부 전체 기관의 경우 혈관계에 고정제를 관류하여 (관류고정) 하기도 합니다. 일부 특수화 조직화학적 방법에서는 때때로 고정제가 증기의 형태로 쓰이는 경우도 있습니다. 예를 들어 파라 포름알데히드와 오스뮴 테트록 사이드는 동결 건조된 조직을 증기고정 할 때 사용될 수 있습니다.
고정액 은 하나의 고정제가 물이나 알코올 같은 용매, 혹은 일반적으로 산도(pH)를 안정화하기 위한 완충 용액에 용해되어 사용될 수 있습니다. 일부 많이 사용되는 고정액은 여러 가지의 다른 고정제들이 조합되어 있는데, 이는 한 고정제의 결함이 다른 고정제를 추가함으로써 보정될 수 있기 때문입니다. 예를 들어, 아세트산은 에탄올과 같은 다른 고정제가 수축을 일으키는 것을 보정하기 위해 일부 제제에 포함되어 있습니다. 5
고정의 이론적 근거
고정은 “복잡한 일련의 화학적 사건들”로 간주될 수 있습니다.6현재 우리는 이러한 “사건들” 중 일부를 정의할 수 있지만, 고정 과정 중에 일어나는 일들의 상당 부분에 대한 이해는 여전히 완전하지 않다. 세포 및 세포 외 성분은 펩타이드와 단백질, 지질과 인지질 (막), 탄수화물과 탄수화물 복합체, 다양한 종류의 RNA와 DNA 등을 포함하고 있습니다. 이러한 성분들이 고정 과정 중에 어떻게 반응하는 가는 고정의 종류, 사용된 고정제와 고정 조건에 따라 다르다. 어떤 조직 성분들은 화학적으로 고정제와 반응하고 교차결합을 통해 안정화되어 보존되며, 다른 성분들은 고정의 영향은 받지 않지만 고정된 성분들에 의해 세포나 조직 내에 갇힐 수 있습니다.
고정제의 분류 및 고정의 기전
전통적으로 고정제는 용액 내 수용성 단백질에 대한 영향을 기준으로 “응고제” 또는 “비응고제”로 불렸다. 7응고제는 단백질 가닥의 투과성 섬유주를 초래하는 것으로 알려졌던 반면 자연적으로 부가적인 비응고제는 덜 투과적인 겔을 생산하는 광범위한 교차결합을 형성합니다. 이러한 용어들은 현대 조직학 문헌에서 여전히 보이긴 하지만, 최근에는 더욱 체계적인 방법이 분류에 사용되고 있습니다. 2
단백질과 단백질 복합체의 고정에 중요한 다음과 같은 두 가지 주요 기전들이 있습니다: 변성, 그리고 첨가 및 교차결합 형성.
변성: 변성의 영향은 가장 흔히 알코올이나 아세톤 같은 탈수제에 의해 유도된다. 이러한 시약들은 세포와 조직에서 유리 수분을 제거하고 교체하며, 소수성 결합을 불안정화하여 단백질의 3차 구조에 변화를 일으킨다. 단백질 분자 내부에서 흔히 발견되는 소수성 부위는 물의 반발력에 의해 방출되며 더 큰 부위를 자유롭게 차지하게 된다. 단백질의 친수성 부위에서는 물 분자가 수소 결합에 의해 느슨하게 결합하고 물의 제거 또한 이 결합을 불안정화 시킵니다. 단백질 분자들의 입체 형태에서 발생하는 변화는 수용성 단백질을 불용성으로 바꿔 단백질 용해도에 변화를 일으키는데, 이는 단백질이 수용성 환경에 되돌아가면 대체로 불가역적인 변화입니다. 2, 7
첨가 및 교차결합 형성: 비 응고 고정제는 단백질과 다른 세포와 조직 구성 성분들과 화학적으로 반응하여 첨가하고 분자 내 및 분자 간 교차결합을 형성함으로써 결합합니다. 이러한 제제들은 반응성 화합물이기 때문에 조직 내 다양한 화학 구조에 결합하여 종종 결합 부위의 전하량에 영향을 미친다. 이는 이어지는 특정 단백질의 염색 특성에 영향을 미칠 수 있고 분자의 입체 형태 또한 변형시켜 용해도를 바꿀 수 있습니다.
예를 들어 포름알데히드로 고정된 조직은 에오신으로 염색이 잘 안 되는데, 이는 포름알데히드가 메틸렌 브리지를 형성하기 위해 아미노기와 광범위하게 반응하고 이에 따라 에오신과 같은 음전하의 색소 분자들이 아미노기와 더 결합할 수 없기 때문입니다. 첨가 고정제가 교차결합을 형성하는 정도는 상당히 다양합니다. 예를 들어 글루타르 알데히드는 포름알데히드보다 교차결합을 형성하는데 더 효과적입니다. 8 이것은 왜 글루타르알데히드가 세포의 미세구조를 효과적으로 보존하고 전자현미경 검사용으로 선택되는 고정제인지 설명합니다. 또한 이는 왜 글루타르알데히드로 고정된 조직이 전통적인 염색법으로 염색이 잘 안 되는지 설명합니다. 조직 고정에서의 화학 반응은 포름알데히드와 같은 일부 고정제의 경우 꽤 이해가 잘 되지만, 일부 다른 고정제들과 관련된 기전에 대한 우리의 지식은 아직 불완전합니다.
면역조직화학에서 항원복원 방법은 고정에서의 몇몇 반응들이 (특히 포름알데히드 반응들이) 가역적이라는 것을 보여줬으나, 여러 고정제 사용시 항원 복원의 질에는 상당한 차이가 나타난다. 항원성의 보존은 고정제를 선택하는 데 있어 매우 중요한 고려사항입니다.

발표자 소개

Geoffrey Rolls is a Histology Consultant with decades of experience in the field. He is a former Senior Lecturer in histopathology in the Department of Laboratory Medicine, RMIT University in Melbourne, Australia.
참조 문헌
- Drury RAB, Wallington EA. Carleton's histological technique. 5th ed. New York: Churchill Livingstone, 1980.
- Eltoum I, Fredenburgh J, Myers RB, Grizzle WE. Introduction to the theory and practice of fixation of tissues. J Histotechnol 2001;24;173 -190.
- Winsor L. Tissue processing. In Woods A and Ellis R eds. Laboratory histopathology. New York: Churchill Livingstone, 1994;4.2-1 - 4.2-39.
- Williams JH, Mepham BL, Wright DH. Tissue preparation for immunocytochemistry. J Clin Pathol 1997;50;422-428.
- Leong AS-Y. Fixation and fixatives. In Woods AE and Ellis RC eds. Laboratory histopathology. New York: Churchill Livingstone, 1994;4.1-1 - 4.1-26.
- Hopwood D. Fixation and fixatives. In Bancroft J and Stevens A eds. Theory and practice of histological techniques. New York: Churchill Livingstone, 1996.
- Carson FL. Histotechnology. 2nd ed. Chicago: ASCP Press, 1997.
- Pearse AGE. Histochemistry, theoretical and applied. London: Churchill Livingstone, 1980
Related Content
라이카 바이오시스템즈 Knowledge Pathway 콘텐츠는 에서 이용할 수 있는 라이카 바이오시스템즈 웹사이트 이용 약관의 적용을 받습니다. 법적고지. 라이카 바이오시스템즈 웨비나, 교육 프레젠테이션 및 관련 자료는 특별 주제 관련 일반 정보를 제공하지만 의료, 규정 또는 법률 상담으로 제공되지 않으며 해석되어서는 안 됩니다. 관점과 의견은 발표자/저자의 개인 관점과 의견이며 라이카 바이오시스템즈, 그 직원 또는 대행사의 관점이나 의견을 나타내거나 반영하지 않습니다. 제3자 자원 또는 콘텐츠에 대한 액세스를 제공하는 콘텐츠에 포함된 모든 링크는 오직 편의를 위해 제공됩니다.
모든 제품 사용에 다양한 제품 및 장치의 제품 정보 가이드, 부속 문서 및 작동 설명서를 참조해야 합니다.
Copyright © 2025 Leica Biosystems division of Leica Microsystems, Inc. and its Leica Biosystems affiliates. All rights reserved. LEICA and the Leica Logo are registered trademarks of Leica Microsystems IR GmbH.



