
Fijación y Fijadores (3): agentes de fijación distintos de los aldehídos comunes

Además del formaldehído y el glutaraldehído, analizados anteriormente, se han utilizado otros reactivos para la fijación, a veces en solución simple pero a menudo combinados con otros agentes en forma de fijadores compuestos. Las más importantes de estas se comentan aquí en la Parte 3 de la serie de Fijadores y Fijadores.
Acroleína
La acroleína o aldehído acrílico (H2C=CH.CHO) reacciona con las macromoléculas de forma similar a los enlaces cruzados reversibles que forman el formaldehído. Se ha demostrado que produce más enlaces cruzados que el formaldehído. La acroleína reacciona con los ácidos grasos a través de su doble enlace. Aunque la acroleína penetra en el tejido rápidamente y es extremadamente reactiva, no ha sido aceptada de forma generalizada porque es desagradable de usar (tiene un potente agente lagrimal), es inestable a un pH alcalino y forma fácilmente polímeros. Se ha utilizado principalmente para la histoquímica enzimática y para la fijación de material vegetal. Después de la fijación, los grupos de carbonilo residual en el tejido provocarán la tinción de fondo con técnicas como el PAS.1-3
Glioxal
El glioxal o diformil (OHCCHO) es un aldehído bifuncional que reacciona de manera similar al formaldehído y produce una imagen morfológica similar. Cada uno de los grupos aldehídos es potencialmente reactivo y se pueden formar enlaces cruzados. El glioxal es el principal ingrediente en varios fijadores patentados particularmente aplicables a la fijación con microondas, así como para el trabajo rutinario. Se denomina comúnmente “sustituto del formol”, ya que su uso se considera menos peligroso que el del formaldehído al no producir prácticamente vapores a temperatura ambiente con una presión de vapor extremadamente baja. Aunque es irritante y potencialmente sensibilizador al contacto con la piel, actualmente no está clasificado como carcinógeno, aunque se proporcionan advertencias sobre sus posibles efectos mutagénicos. Reacciona con el ADN formando aductos de forma inestable y reversible. Parece ser biodegradable, por lo que su eliminación será más fácil que la del formol. 2, 4, 5
Tetróxido de osmio
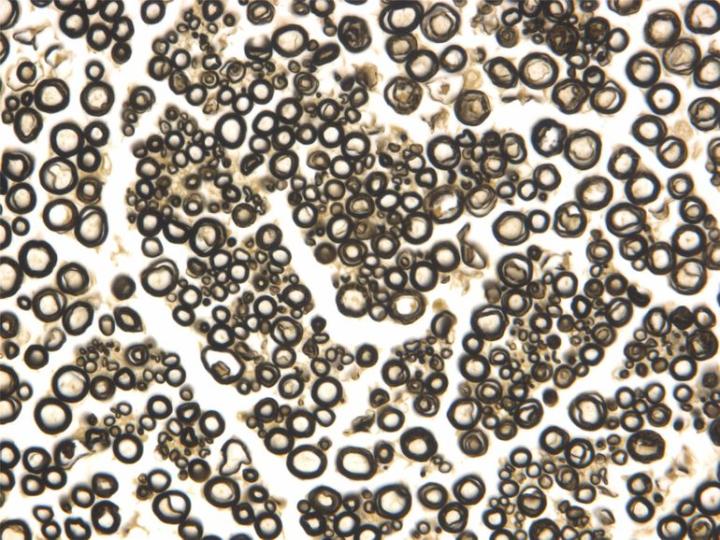
El tetróxido de osmio (OsO4) es un sólido cristalino volátil altamente tóxico que se suministra en ampollas selladas. Debido a su volatilidad, debe manipularse con mucho cuidado bajo una campana extractora, ya que afectará fácilmente a la conjuntiva del ojo y a la mucosa nasal.6 Es soluble en disolventes polares y no polares y reacciona con las cadenas laterales de proteínas que forman enlaces cruzados. Las reacciones de fijación más importantes del tetróxido de osmio son aquellas que implican enlaces insaturados de lípidos y fosfolípidos, ya que es uno de los pocos fijadores que estabiliza los lípidos. Durante la fijación, el tetróxido de osmio se reduce a óxidos inferiores, que son negros e insolubles y se depositan en los tejidos, especialmente en las membranas. El osmio es un metal pesado que dispersa electrones y, por tanto, añade densidad de electrón a la imagen del microscopio electrónico.7, 8 También se puede utilizar como tinción en bloque para mostrar lípidos (particularmente fibras nerviosas mielínicas) a nivel del microscopio óptico. Por lo general, se utiliza a aproximadamente el 1 % p/v como fijador secundario especializado para microscopía electrónica y para preparaciones de fibras nerviosas separadas.9
Carbodiimidas:
Las carbodiimidas (RN=C=NR’) son compuestos muy reactivos que reaccionan con una gama de grupos funcionales. Las reacciones pueden mejorarse o bloquearse selectivamente eligiendo un tipo particular de carbodiimida, pH, temperatura o catalizador. Debido a que los enlaces peptídicos pueden formarse como un resultado de las reacciones de fijación y posteriormente pueden romperse selectivamente usando proteasas, se cree que este grupo de compuestos tiene cierto potencial para su uso en inmunohistoquímica así como para histología rutinaria. Las carbodiimidas ya se utilizan para la preparación de inmunógenos.2
Otros agentes de enlaces cruzados
Los diimidoésteres son compuestos solubles en agua que forman enlaces cruzados con grupos amino de proteínas y se han utilizado para microscopía electrónica e inmunohistoquímica. Las cloro-s-triazinas (cloruro cianúrico) se han utilizado para las mucinas de las glándulas salivales y la inmunofluorescencia. Los diisocianatos se han utilizado para fijar marcas fluorescentes en las proteínas, mientras que el dietilpirocarbonato (DPC) reacciona con los residuos de triptófano y se ha utilizado como fijador en fase de vapor para tejido liofilizado. Se ha propuesto como fijador en una solución tampón adecuada para muestras pequeñas. Las maleimidas parecen formar algunos enlaces cruzados con proteínas y la benzoquinona reacciona con aminas, aminoácidos y péptidos y se ha utilizado para fijar péptidos en tejidos endocrinos para la inmunohistoquímica.2, 3
Cloruro de mercurio
El cloruro de mercurio (HgCl2) fue uno de los primeros reactivos utilizados para la fijación tisular. En la literatura más antigua se las denominaba “sublimado corrosivo”, un nombre apropiado, ya que es un químico corrosivo que reacciona con metales, incluido el acero inoxidable de los instrumentos de disección. Aunque los mecanismos por los que fija el tejido no se entienden por completo, se sabe que reacciona con aminas, amidas, aminoácidos y grupos sulfhidrilos, siendo estos últimos prominentes en su reacción con cisteína, con la que se cree que produce enlaces cruzados. Es un poderoso coagulante proteico que deja el tejido en un estado que produce una fuerte tinción con colorantes ácidos. Reacciona con los residuos de fosfato de los ácidos nucleicos y fija de forma efectiva las nucleoproteínas. Es por este motivo que es el componente principal de los fijadores formulados como B-5 y la solución de Helly, los fijadores recomendados cuando se requiere una conservación nuclear de alta calidad (p. ej., trefinas de médula ósea).
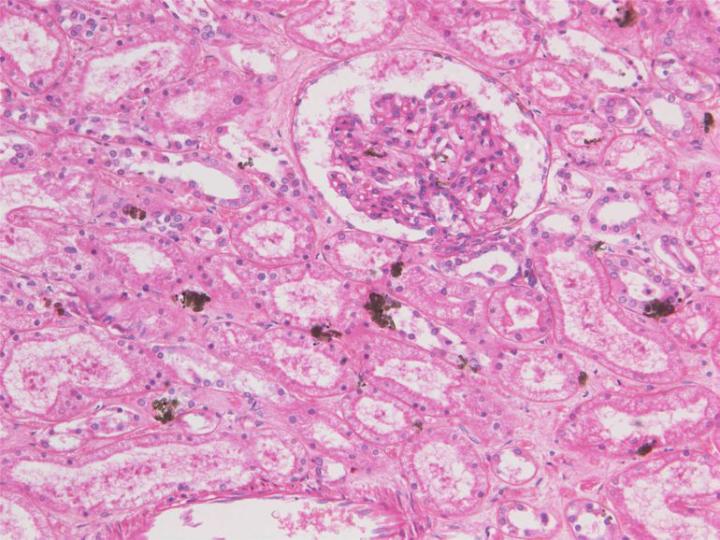
El uso de fijadores que contienen cloruro de mercurio tiene varias desventajas. Aparte de la naturaleza corrosiva del cloruro de mercurio, el mercurio es altamente tóxico, se puede absorber a través de la piel y es un veneno acumulativo. En la mayoría de los países existen normas estrictas sobre la eliminación del mercurio y compuestos que contienen mercurio. Durante la fijación con fijadores que contienen cloruro de mercurio, se deposita aleatoriamente en los tejidos un pigmento de artefacto cristalino o amorfo de color marrón verdoso. El tratamiento de las muestras con yodo (yodo de Lugol) durante el procesamiento o las secciones antes de la tinción producirá yoduro de mercurio, que puede eliminarse de los tejidos. Después, con un tratamiento con tiosulfato sódico se puede eliminar el yodo residual. Los fijadores basados en cloruro mercúrico tienden a penetrar de forma deficiente y, si la fijación es prolongada, los tejidos se endurecen mucho y son propensos a encoger durante el procesamiento.6, 7
En los últimos años se han introducido varias sales metálicas como sustitutos del cloruro de mercurio, incluidas las sales de zinc y bario. El cloruro de zinc y el sulfato de zinc se han aceptado ampliamente como fijadores adecuados y ahora hay muchos sustitutos B-5 patentados disponibles.6
Sales de zinc
El sulfato de zinc (ZnSO4) y el cloruro de zinc (ZnCl2) se utilizan como sustitutos del cloruro de mercurio en una serie de fijadores formulados y patentados, siendo el sulfato más popular porque es potencialmente menos corrosivo que el cloruro, que según se ha informado, ha causado problemas en los procesadores de tejidos6 (consulte la Parte 4). Las sales se añaden a las soluciones de formol al 10 % (acuosas o alcohólicas, tamponadas o no tamponadas), a una concentración de aproximadamente 1 %, pero se han notificado algunos problemas con la precipitación de zinc o sales tampón durante la preparación. Las sales de zinc reaccionan con varios grupos finales de tejido, incluidos amino, carboxilo y sulfhidrilo, formando productos de reacción reversibles, algunos de los cuales pueden eliminarse con un lavado con citrato o EDTA. Parece que el zinc mejora la fijación y la tinción, especialmente de los núcleos, de manera similar al cloruro de mercurio. Se afirma que tiene ventajas en la conservación de la inmunorreactividad en comparación con el formol solo, lo que evita la necesidad de obtener antígenos para algunos epítopos. Las sales de zinc son mucho menos tóxicas que las sales de mercurio y la eliminación de las soluciones de zinc no debería suponer ningún problema2, 6.
Ácido pícrico
El ácido pícrico o trinitrofenol (C6H2(NO2)3OH) es una sustancia cristalina de color amarillo brillante que debe almacenarse húmeda con agua para evitar el riesgo de explosión por percusión o calentamiento de la sustancia seca. Debe conservarse en un recipiente herméticamente cerrado y comprobarse regularmente para comprobar que está húmedo.10 Se puede añadir agua destilada si parece que se está secando. Para la fijación, siempre se utiliza en combinación con otros agentes (consulte la Parte 4: soluciones de Bouin y Hollande). Además de ser un componente de los fijadores, el ácido pícrico se utiliza como colorante ácido en varias tinciones (p. ej., en la solución de Van Gieson para la tinción muscular). Se aplica un color amarillo a los tejidos durante la fijación y, debido a su naturaleza ácida, el ácido pícrico residual debe retirarse de los tejidos con etanol al 70 % antes de procesarlos. Si el ácido pícrico residual permanece en los bloques de tejido después del procesamiento, las características de tinción del tejido se verán afectadas y se deteriorarán con el tiempo.
El ácido pícrico es un fijador coagulante que cambia las cargas en las cadenas laterales ionizables de proteínas y altera los enlaces electrostáticos y de hidrógeno. Forma sales (picratos) con grupos básicos de proteínas que causan coagulación. Parece que no fija lípidos ni la mayoría de los carbohidratos, pero se recomienda como componente de los fijadores utilizados para preservar el glucógeno. El ácido pícrico puede hidrolizar los ácidos nucleicos, por lo que debe evitarse si se debe mostrar el ADN o el ARN. El ácido pícrico disolverá los pequeños depósitos de calcio en las muestras. Durante el procesamiento de los tejidos fijados en reactivos que contienen ácido pícrico se produce una contracción considerable.6, 7, 11
Dicromato potásico
El dicromato de potasio (K2Cr2O7) se comporta como no coagulante a menos que se utilice con un pH de < 3,4 - 3,8, donde reacciona como el ácido crómico, es decir, como coagulante. Es un componente de varios fijadores compuestos (consulte la Parte 4: soluciones de Zenker y Helly). Se cree que las reacciones de fijación implican la oxidación de proteínas con la interacción de iones cromato reducidos que forman algunos enlaces cruzados, cuya extensión viene determinada por el pH del fijador. Se sabe que los iones de cromo reaccionan con las cadenas laterales carboxilo e hidroxilo de las proteínas. Deja grupos amino disponibles y, por tanto, favorece la tinción con colorantes ácidos. El cromato reaccionará con los lípidos insaturados, haciéndolos insolubles, siendo por este motivo que se considera un buen fijador para las mitocondrias. Por lo general, se recomienda lavar bien en agua los tejidos fijados en un fijador que contenga cromato antes del procesamiento para evitar la formación de un subóxido de cromato insoluble mediante la reacción del alcohol de procesamiento y la sal del cromato. Tradicionalmente, se utilizaban fijadores con dicromato en métodos histoquímicos para la amina que contenía gránulos “cromafines” de tejidos endocrinos.6, 7, 11
Etanol y metanol
El etanol (CH3CH2OH) y el metanol (CH3OH) se consideran coagulantes que desnaturalizan las proteínas. Sustituyen el agua en el entorno tisular, alterando la unión hidrofóbica y de hidrógeno, exponiendo así los grupos hidrófobos internos de proteínas y alterando su estructura terciaria y su solubilidad en agua. El metanol está más cerca de la estructura del agua que la del etanol, por lo que el etanol interactúa más fuertemente con las áreas hidrofóbicas que el metanol. La fijación comienza a una concentración del 50 al 60 % para el etanol y de >80 % para el metanol. El etanol se utiliza a veces para preservar el glucógeno, pero causará distorsión de los detalles nucleares y citoplásmicos. El metanol se suele utilizar como fijador para películas de sangre y el etanol al 95 % se utiliza como fijador para frotis citológicos, pero ambos alcoholes se suelen combinar con otros reactivos cuando se utilizan como fijadores para muestras de tejido.3, 7, 12
Acetona
La acetona (CH3COCH3) tiene una acción similar al alcohol y se ha utilizado como fijador y deshidratante para el procesamiento de tejidos, especialmente para el procesamiento manual rápido de muestras pequeñas. Está ampliamente recomendada para la fijación como parte de la demostración histoquímica de enzimas, donde se utiliza generalmente en frío (4 °C). Es un disolvente lipídico eficaz con una acción rápida que puede hacer que los tejidos se vuelvan quebradizos. Debido a que es altamente volátil e inflamable, generalmente no se utiliza en procesadores automáticos de tejidos.3, 7
La acetona no debe utilizarse en algunos procesadores de tejidos porque dañará las juntas y otros componentes del equipo.
Ácido acético
El ácido acético (CH3COOH) tiene una acción coagulante con los ácidos nucleicos, pero generalmente no fija proteínas. Se incorpora en fijadores compuestos para ayudar a prevenir la pérdida de ácidos nucleicos y, debido a que hincha el colágeno, contrarresta la contracción causada por otros ingredientes como el etanol. El ácido acético penetra muy rápidamente, pero los fijadores que lo contienen destruyen los glóbulos rojos. 3, 7
About the presenter

Geoffrey Rolls is a Histology Consultant with decades of experience in the field. He is a former Senior Lecturer in histopathology in the Department of Laboratory Medicine, RMIT University in Melbourne, Australia.
Referencias
- Culling CFA, Allison RT, Barr WT. Cellular pathology technique. London: Butterworths, 1985;32.
- Eltoum I, Fredenburgh J, Grizzle WE. Advanced concepts in fixation: 1. Effects of fixation on immunohistochemistry, reversibility of fixation and recovery of proteins, nucleic acids, and other molecules from fixed and processed tissues. 2. Developmental methods of fixation. J Histotechnol 2001;24;201-210.
- Leong AS-Y. Fixation and fixatives. In Woods AE y Ellis RC eds. Laboratory histopathology. New York: Churchill Livingstone, 1994;4.1-1 - 4.1-26.
- Fisher Scientific. MSDS :Glyoxal. 2008; . http://fscimage.fishersci.com/msds/01960.htm; November 22, 2011
- Organización Mundial de la Salud. Concise International Chemical Assessment Document 57 GLYOXAL. 2004; http://whqlibdoc.who.int/publications/2004/924153057X.pdf; November 22
- Carson FL. Histotechnology. 2nd ed. Chicago: ASCP Press, 2007.
- Eltoum I, Fredenburgh J, Myers RB, Grizzle WE. Introduction to the theory and practice of fixation of tissues. J Histotechnol 2001;24;173 -190.
- Bozzola JJ, Russell LD. Electron microscopy: principles and techniques for biologists. Boston: Jones y Bartlett, 1992.
- Lowe J. Techniques in neuropathology. En Bancroft JD y Stevens A eds. Theory and practice of histological techniques. New York: Churchill Livingstone, 1996;373.
- Sigma-Aldrich. MSDS Picric acid solution. 2011;22 de noviembre
- Drury RAB, Wallington EA. Carleton's histological technique. . 5th ed. New York: Churchill Livingstone, 1980.
- Lillie RD, Fullmer HM. Histopathologic technique and practical histochemistry. 4th ed. New York: McGraw-Hill, 1976;45.
Related Content
El contenido de Leica Biosystems Knowledge Pathway está sujeto a las condiciones de uso del sitio web de Leica Biosystems, disponibles en: Aviso legal.. El contenido, incluidos los webinars o seminarios web, los recursos de formación y los materiales relacionados, está destinado a proporcionar información general sobre temas concretos de interés para los profesionales de la salud y no está destinado a ser, ni debe interpretarse como asesoramiento médico, normativo o jurídico. Los puntos de vista y opiniones expresados en cualquier contenido de terceros reflejan los puntos de vista y opiniones personales de los ponentes/autores y no representan ni reflejan necesariamente los puntos de vista ni opiniones de Leica Biosystems, sus empleados o sus agentes. Cualquier enlace incluido en el contenido que proporcione acceso a recursos o contenido de terceros se proporciona únicamente por comodidad.
Para el uso de cualquier producto, debe consultarse la documentación correspondiente del producto, incluidas las guías de información, los prospectos y los manuales de funcionamiento.
Copyright © 2025 Leica Biosystems division of Leica Microsystems, Inc. and its Leica Biosystems affiliates. All rights reserved. LEICA and the Leica Logo are registered trademarks of Leica Microsystems IR GmbH.


